Misure sperimentali e simulazioni al calcolatore per contrastare la crescita delle cellule tumorali
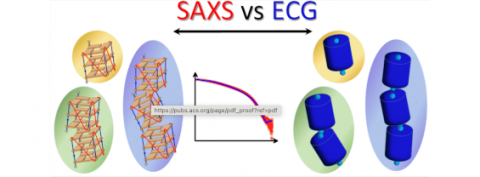
Un nuovo metodo basato sull’applicazione della fisica della materia a sistemi biologici permette di studiare particolari molecole coinvolte nella crescita delle cellule tumorali. Il protocollo messo a punto, frutto della collaborazione fra il Dipartimento di Fisica della Sapienza, il Dipartimento di Fisica e Geologia dell’Università di Perugia e l’Istituto Officina dei Materiali del Cnr, potrà essere applicato tanto per sviluppare farmaci antitumorali di nuova generazione quanto per valutare l’efficacia di quelli esistenti. I risultati dello studio sono stati pubblicati su Journal of American Chemical Society (JACS), che ha anche selezionato un’immagine creata dagli autori come copertina supplementare.
I telomeri sono particolari aree del DNA umano legate a più dell’85% dei tumori maligni e il loro studio potrebbe portare allo sviluppo di farmaci antitumorali di nuova generazione con un ampio spettro d’azione.
Questi elementi si trovano all’estremità dei cromosomi e hanno una funzione protettiva poiché preservano l'integrità del DNA durante i processi di replicazione cellulare, svolgendo un ruolo importante nel processo di invecchiamento cellulare. Ogni volta che una cellula si divide, i telomeri a poco a poco si accorciano sempre di più. Quando diventano troppo corti, la cellula perde la sua capacità di replicarsi correttamente e può entrare in uno stato di invecchiamento o morire. Nel caso delle cellule tumorali di più dell'85% dei tumori maligni, si verifica l'attivazione di un enzima chiamato telomerasi, che mantiene i telomeri più lunghi rispetto alle cellule normali. Ciò conferisce alle cellule tumorali immortalità e la capacità di proliferare in modo illimitato. La stabilizzazione dei G-quadruplex, strutture elicoidali a quattro filamenti che si formano nei telomeri, tramite l'uso di molecole chiamate ligandi, rappresenta un efficace approccio per inibire l'attività della telomerasi e limitare la crescita delle cellule tumorali. Questi ligandi potrebbero quindi fungere da nuovi farmaci per il trattamento del cancro.
La maggior parte delle ricerche attuali si concentra sui G-quadruplex in condizioni ideali, cioè come molecole biologiche che non interagiscono reciprocamente. Tuttavia, in condizioni biologicamente rilevanti, come ad esempio alle estremità dei cromosomi, possono formarsi strutture composte da più unità interagenti di G-quadruplex, note come multimeri.
In uno studio coordinato da Cristiano De Michele del Dipartimento di Fisica della Sapienza, Lucia Comez dell’Istituto Officina dei Materiali del Cnr di Perugia e Alessandro Paciaroni del Dipartimento di Fisica e Geologia dell’Università di Perugia è stato sviluppato un nuovo metodo che consente di ottenere informazioni sulla stabilità di multimeri di G-quadruplex telomerici. I risultati dello studio, pubblicati sulla rivista Journal of American Chemical Society (JACS), potranno essere applicati tanto per sviluppare farmaci antitumorali di nuova generazione quanto per valutare l’efficacia di quelli esistenti. In particolare, i ricercatori hanno utilizzato per la prima volta delle simulazioni “extremely coarse-grained” in cui i G-quadruplex vengono rappresentati con semplici forme geometriche, come cilindri o parallelepipedi. Queste simulazioni non sono particolarmente pesanti e consentono lo studio di migliaia di G-quadruplex interagenti tra di loro, riproducendo così condizioni biologicamente rilevanti. Questo ha permesso un confronto diretto tra i risultati numerici al calcolatore e gli esperimenti effettuati sia presso i nostri laboratori che in centri di ricerca internazionali, fornendo una inedita rappresentazione dei multimeri di G-quadruplex. “In particolare – spiega De Michele - abbiamo studiato come dei ligandi, cioè dei potenziali farmaci antitumorali, agiscano sui G-quadruplex e grazie al nostro innovativo approccio abbiamo potuto capire in che modo risultano efficaci nella loro stabilizzazione”. “Inoltre – aggiunge Paciaroni - nel nostro lavoro definiamo un protocollo che si potrà applicare per lo studio dei G-quadruplex, ma che in futuro potrà anche essere utilizzato per altri sistemi biofisici”. “Questo studio – conclude Comez – rappresenta un notevole passo in avanti nel nostro percorso, iniziato diversi anni fa, per comprendere le proprietà elusive di questi sistemi biologici altamente complessi”.
Autori:
Benedetta Petra Rosi, Valeria Libera, Luca Bertini, Andrea Orecchini, Silvia Corezzi, Giorgio Schiro, Petra Pernot, Ralf Biehl, Caterina Petrillo, Lucia Comez, Cristiano De Michele, Alessandro Paciaroni
Rivista:
Journal of the American Chemical Society (JACS)
